自然-通信的新成果揭示了焦虑障碍的新机制
研发家
|
2025-05-28
34
近日,康复大学生命科学与健康学院与青岛大学基础医学院联合研究团队在国际顶级期刊《自然-通信》上发表了重要研究成果。这项研究首次澄清了生长激素促分泌素受体1a(GHS-R1a),通过调节下丘脑神经元兴奋性参与焦虑行为发展的分子机制,为焦虑障碍的治疗提供了新的目标。
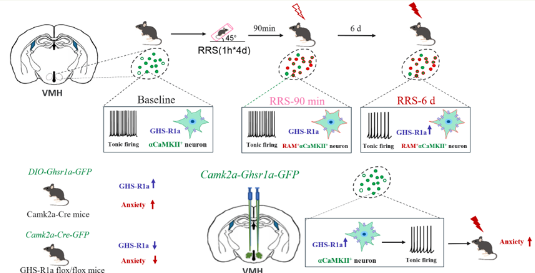
焦虑症是世界上最常见的精神疾病之一,但其神经机制尚未得到充分阐明。
研究小组发现,在压力下,下丘脑腹部的核神经元活性明显增加,GHS-R1a信号通道的上调会降低这种神经元的兴奋性,进而促进焦虑。GHS-R1通过光遗传学和化学遗传技术精确控制a,实验动物的焦虑表现可以得到有效缓解或加重,这证明了该通道的因果作用。这一发现不仅揭示了焦虑形成的细胞分子机制,也表明GHS-R1a可能成为药物开发的新目标。
慢性压力是焦虑的主要诱因。虽然此前的研究发现代谢激素生长激素释放肽及其受体GHS-R1a参与情绪调节,但其具体作用路径仍不明确。该研究创新性地聚焦于压力反应的关键脑区下丘脑腹内侧核,结合电生理记录、行为分析和神经调节技术,系统地分析了GHS-R1a信号通过阳性神经元影响焦虑行为的完整链条。实验数据显示,抑制GHS-R1a活动可以显著改善焦虑行为,而激活该路径则产生相反的效果,为临床干预提供了明确的方向。
研究人员指出,这一发现对于创伤后应激障碍等疾病具有重要的应用前景。未来,焦虑症状的精确控制可以通过开发GHS-R1a特异性调节剂来实现。目前,团队正在进一步探索该机制在不同类型焦虑障碍中的普遍性,并推动转型医学研究。
这一结果得到了国家自然科学基金等项目的支持,相关技术已经申请了发明专利,为精神疾病治疗策略的创新奠定了科学基础。
赞一个
31
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权
最新文章
NEW
热点资讯
HOT
学术资源免费领取
加微信领取20G科研大礼包!
更有众多热门
更有众多热门



















