科学家们开发了一种新的吸入药物载体,帮助治疗呼吸道疾病
中国科学院上海药物研究所研究员张继稳、副研究员伍丽团队和合作伙伴探索了羟丙基-贝塔-环糊精(HCD)超多组分金属有机骨架形成(HCD-pMOFs)对其作为吸入药物输送载体的应用潜力进行评估,证明HCD-pMOFs具有吸入药物输送载体的潜力,有望成为治疗呼吸道疾病的新载体材料。最近,《碳水化合物》发表了相关研究。
有机金属骨架(MOFs)具有比表面积大、粒径可控以及可功能化等优势,近年来在药物载体领域备受关注。由天然环糊精和碱金属离子自组装形成的环糊精有机金属骨架(CD-MOFs),晶态MOFs是典型的结构规则,配体单一。(cMOFs)。CD-MOFs具有药物高效负载能力、外形规则、粒径可控等特点,在吸入制剂载体领域显示出应用潜力。但是,到目前为止,所有的CD-MOFs都是由单一类型的天然环糊精组成的。HCD是一种环糊精衍生物,广泛应用于药物和食品领域,其分子中的羟丙基在替代位置和数量上具有高度随机分布的特点。
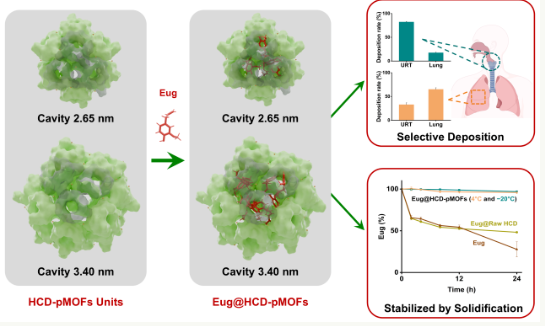
研究小组提出了以HCD为配体的“多分散多组分MOFs”概念,并结合钠离子(Na+),设计非晶态HCD。-pMOFs。观察显示,HCD-PMOFs具有规则的球形、可控的粒径和分级孔结构,其中HCD和Na+通过配位构建了2.65纳米和3.40纳米孔径的空腔。
此外,研究人员讨论了HCD和Na+之间的多配位模式,并提出了HCD-pMOFs的超分子结构单元假设。研究人员将丁香酚作为挥发性成分(Eug)HCD-pMOFs作为一种模型药物,能有效地将Eug包裹在其超分子结构单元中,使Eug能以纳米球形式固化,提高热稳定性。
另外,研究人员利用两种冷却工艺,分别获得了两种不同粒径的HCD。-pMOFs。其中,4℃冷却过程中获得的小颗粒主要沉积在肺部,而-20℃冷却过程中获得的大颗粒则表现出较好的上呼吸道沉积,表现出基于颗粒尺寸的区域靶向优势。大鼠体内的安全性评价证实,吸入HCD-pMOFs时没有明显的组织刺激,生物安全性好。
赞一个
更有众多热门



















