研究人员揭示了RNA聚合酶III转录的动态过程
复旦大学研究员徐彦辉、年轻研究员陈曦子团队重建了人源RNA聚合酶PolPol III转录开始的完整动态过程揭示了Pol驱动Pol的转录因子与聚合酶催化活性的协同驱动。为了了解真核短链非编码RNA的调控,III从转录开始向延伸过渡的分子机制提供了关键的结构基础。6月4日,《自然》发表了相关研究。
聚合酶RNA(RNAPs)是转录的关键酶,负责将DNA上的遗传信息转录为RNA。在哺乳动物中,聚合酶RNA进化出3种功能分化的方式,即Pol I、Pol II和Pol III。其中,Pol II负责转录编码蛋白质的mRNA,与基因表达调节密切相关,是转录研究的重点对象。Pol III主要转录各种短链非编码RNA,在蛋白质合成、RNA剪切和细胞周期调节中起着关键作用。系统分析转录开始过程中的动态变化,尤其是从转录开始到延伸的关键转折机制,是对转录调控核心内容的深刻理解,也是目前最具挑战性的研究难点之一。
研究小组参照并优化了早期的Pol II研究方法设计了一种策略,可以捕捉转录开始向延伸转换过程中的关键中间状态。研究人员首先构建了多个启动子DNA模板,并将这些DNA模板与通用转录因子(GTFs)以及Pol III共同组装,启动体外转录反应,然后获得多个不同阶段的转录复合物。(TC)。
此外,研究小组利用冷冻电镜单颗粒技术对7个高分辨率PolPol进行了分析 III-TC结构。数据显示,Pol II与线粒体RNAP相比,Pol III转录开始向延伸转换所需的RNA链长度较短,仅为6个核苷酸。研究小组得出结论,可能与Pol 在高效生成短链非编码RNA中,III负责的模板类型及其功能要求密切相关。
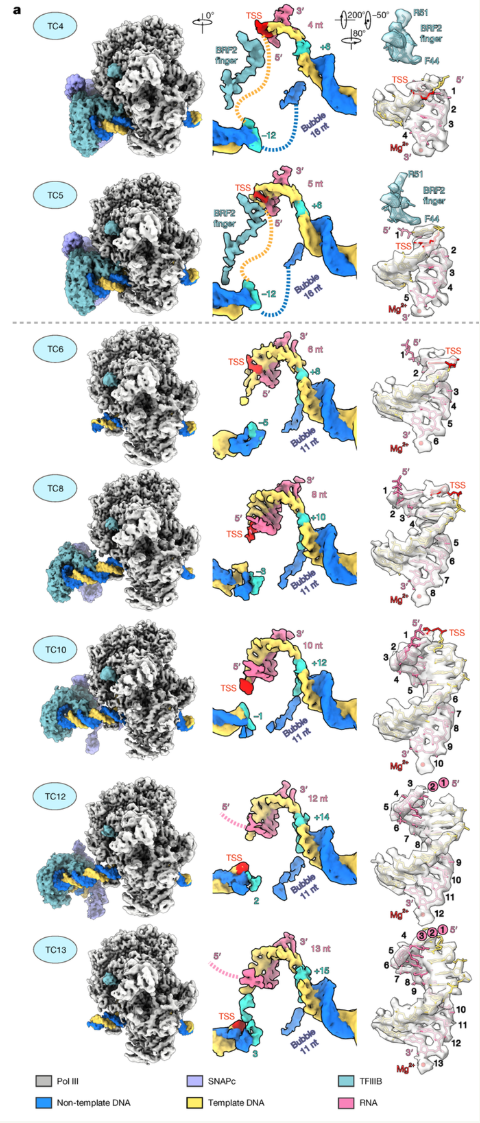
研究小组获得的另一个重要发现是关于转录“重新开始”的结构证据。尽管Pol III进入延伸状态后,与通用转录因子的直接相互作用被打破,但这些因素仍然稳定地结合在启动子的上游区域,支持转录再启动系统的存在。研究发现,Pol可能是在初始阶段完成转录延伸转换和快速再启动机制。在实施高频转录任务时,III采用的策略。
值得一提的是,研究小组在这项研究中建立了一种全新的转录起始活性检测方法,不需要同位素。该方法灵敏度高,安全微毒,操作方便,适用于常规分子生物实验室,大大提高了转录研究的效率和准确性。
赞一个
更有众多热门



















