科学家们开发了一种新的单细胞谱系跟踪技术
研发家
|
2025-05-07
21
一月二十八日,中国科学院广州生物医学与健康研究所研究员彭广敦团队在《细胞-报告》中(Cell Reports)公布重要研究成果。在国家重点研发计划、国家自然科学基金等项目的支持下,他们成功地开发了一个名为“DuTracer新型单细胞谱系示踪技术。
“‘DuTracer论文通讯作者彭广敦表示,该技术通过将CRISPR-Cas9和Cas12a巧妙地结合在一起,显著提高了细胞谱系跟踪的精度和深度,为分析胚胎发育、器官再生和疾病机制提供了新的工具。
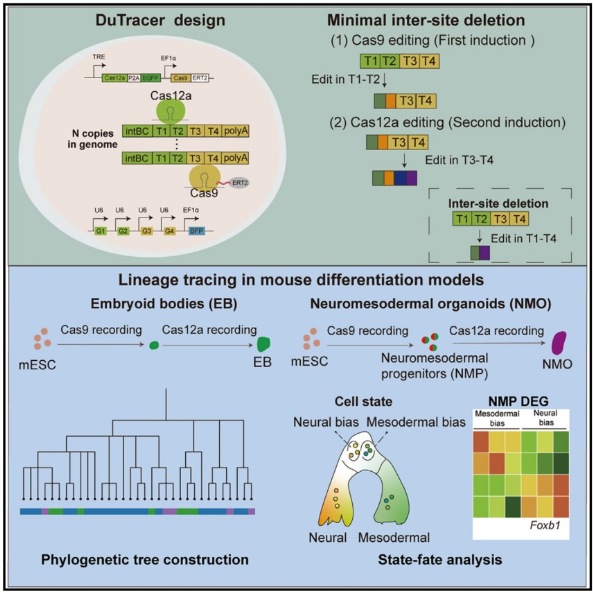
在生物学中,细胞谱系示踪类似于绘制“细胞家族树”,可以追溯细胞从起源到分化的完整过程。传统的方法往往由于技术限制而导致信息记录不完整。虽然基于CRISPR的基因编辑技术提高了分辨率,但存在“在靶点之间删除大片段”的问题——这就像在记录家族历史时丢失关键的跨代信息一样。
“DuTracer“创新在于同时使用Cas9和Cas12a两种核酸酶,通过调整其激活时间,有效防止多目标同时编辑造成的显示信息丢失。实验表明,该技术大大降低了小鼠胚胎干细胞和类器官模型中的有害删除事件,记录了更深层次的细胞分裂,可以更准确地恢复细胞分化路径。
在HEK293T细胞和小鼠器官中,彭广敦团队验证了这一点。DuTracer“性能。数据显示,该技术不仅可以区分心脏细胞(如第一心域和第二心域)的差异来源,还首次揭示了“神经中胚层前体细胞”(NMPs)“分化偏好。例如,转录因子Foxb1被确认为促进NMP向神经谱系分化的关键调节因素。它的缺失会阻碍神经发育,增强中胚层的特征。
“‘DuTracer“它不仅适用于胚胎发育研究,也适用于分析癌症转移和器官再生等复杂过程。”彭广敦指出,该团队计划进一步优化技术,探索其在人体器官和动物模型中的应用。
赞一个
15
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权
最新文章
NEW
热点资讯
HOT
学术资源免费领取
加微信领取20G科研大礼包!
更有众多热门
更有众多热门



















