开拓克罗恩病药治疗新方向研究
研发家
|
2025-05-14
21
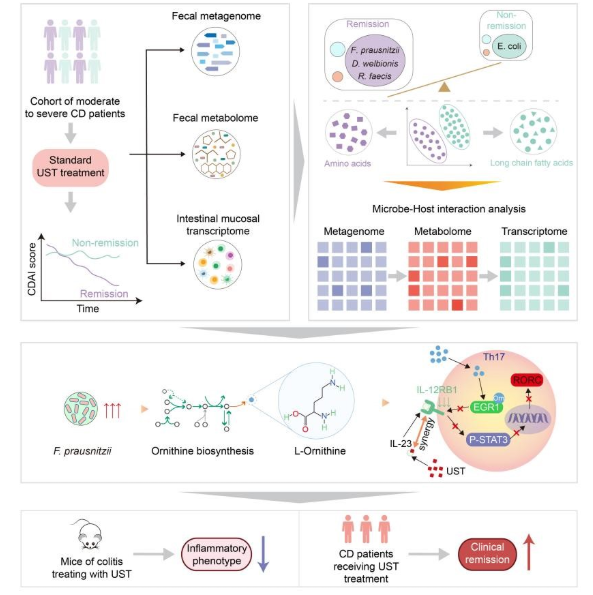
上海交通大学医学院附属仁济医院消化科研究员洪洁团队及其合作伙伴首次表示,以普拉梭菌为代表的肠道微生物驱动的L-鸟氨酸生物合成可以显著提高乌司奴单抗的临床疗效,为克罗恩疾病的治疗提供了新的生物标志,开辟了乌司奴单抗联合药物治疗的新方向。2月19日,《细胞代谢》发表了相关研究。
克罗恩病是一种慢性炎性肉芽肿,诱因不明,影响整个消化道,可引起肠道狭窄、穿孔等症状,有高危复发的倾向。肠道微生物在炎症性肠道疾病的发展中起着至关重要的作用。他们通过复杂的代谢活动与宿主建立动态共生关系,调节宿主的正常生理功能和疾病进程。
研究小组分析了85名接受乌司奴单抗治疗的克罗恩患者的粪便微生物群,发现临床缓解患者的微生物群更加多样化,各种有益菌群明显增多,与炎症指标明显相关。
根据多组学联合分析数据,由肠道菌群驱动产生的L-鸟氨酸与乌司奴单抗具有良好的协同抗炎能力,这一结果在各种肠炎动物模型中得到了验证。机制研究表明,L-在Th17细胞中,鸟氨酸可结合EGR1转录因子,从而抑制其对IL-12RB1受体基因的转录激活,阻隔IL-23/IL-Th17细胞促炎活性减弱,12RB1/TYK2/STAT3信号级联反应。
进一步,研究小组进行了前瞻性临床试验,发现乌司奴单抗耐药的克罗恩患者在使用乌司奴单抗和L-鸟氨酸治疗后,HBI分数和钙卫蛋白水平下降,内镜缓解率和组织分数明显提高。研究结果表明,乌司奴单抗和L-鸟氨酸可能为克罗恩患者提供了新的治疗策略,特别是对于乌司奴耐药患者,这种联合方案可能会为其恢复疗效提供新的希望。
赞一个
16
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权
最新文章
NEW
热点资讯
HOT
学术资源免费领取
加微信领取20G科研大礼包!
更有众多热门
更有众多热门



















