一周连发2篇大子刊!曹雪涛院士之子,曹云龙研究员再取新进展
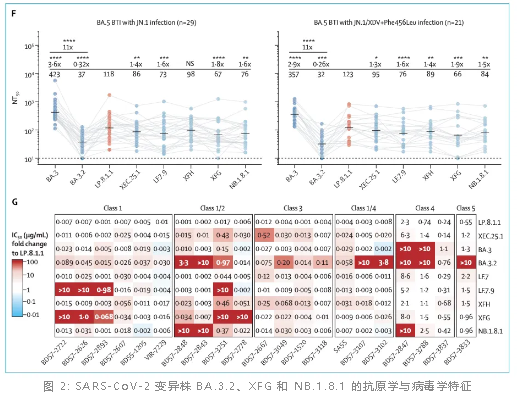
2025 年 6 月 5 日,北京大学生物医学前沿创新中心/昌平实验室/北大-清华生命科学联合中心曹云龙研究员团队在 The Lancet Infectious Diseases 上发表了题为「Antigenic and virological characteristics of SARS-CoV-2 variants BA.3.2, XFG, and NB.1.8.1」的研究性文章,该研究揭示了 SARS-CoV-2 变异株 BA.3.2、XFG 和 NB.1.8.1 的抗原性和病毒学特性,包括它们对疫苗诱导抗体的中和敏感性、与人类 ACE2 受体的结合亲和力以及感染效率,为理解病毒变异机制和评估疫苗有效性提供了重要科学依据。

该研究提出了针对流行的高频突变病毒,通过预测病毒进化热点,快速准确筛选出广谱中和抗体的策略。通过对大流行早期数据以及原始株突变的回顾性研究,该工作显示这一基于精准突变预测的策略能显著富集真正抵抗未来逃逸突变的广谱中和抗体,将发现广谱中和抗体的机会从大约 1% 提高到 40%,并进一步发现了来自原始株康复者的广谱中和抗体 BD55-1205。
该抗体不但能中和所有现存的 SARS-CoV-2 突变株,与相同表位的其他抗体相比还对表位上的逃逸突变具有很强的抵抗能力,具有开发为新一代 SARS-CoV-2 广谱中和抗体药物的潜力。
2025 年 6 月 10 日,曹云龙研究员联合美国莫德纳公司 Laura M. Walker、中国科学院生物物理研究所王祥喜共同通讯在 Nature Microbiology 上发表了题为「Viral evolution prediction identifies broadly neutralizing antibodies to existing and prospective SARS-CoV-2 variants」的研究性文章,研究通过病毒进化预测和深度突变扫描技术,成功识别出能够广泛中和现有及潜在SARS-CoV-2变体的单克隆抗体(mAbs)。该方法显著提高了早期疫情中识别XBB.1.5毒株有效bnAbs的概率。其中,BD55-1205抗体对所有测试变体均表现出强大的中和活性,并通过冷冻电镜结构分析揭示了其广泛的反应性机制。此外,利用mRNA脂质纳米颗粒递送编码BD55-1205 IgG的mRNA,在小鼠体内实现了高效的中和抗体滴度。这项研究结合了病毒进化预测与mRNA递送技术,为快速开发针对SARS-CoV-2及其他冠状病毒的下一代抗体对策提供了新途径。


曹云龙,北京大学生物医学前沿创新中心(BIOPIC)研究员、助理教授,北大-清华生命科学联合中心研究员,北京昌平实验室领衔科学家,国家优秀青年科学基金获得者。入选《Nature》杂志2022年度十大人物(Nature's 10)。
2014年毕业于浙江大学竺可桢学院物理学专业,2019年获得哈佛大学化学博士学位。实验室主要围绕病毒B细胞免疫应答、抗体药物设计及疫苗研发等开展了系统性研究,其中新冠中和抗体药物研制、新冠体液免疫响应特征和新冠突变免疫逃逸机制的创新性研究结果为抗击疫情作出了突出贡献。以第一作者、通讯作者在Nature(6篇)、Cell(3篇)、The Lancet Infectious Diseases(4篇)等期刊上发表多篇相关研究文章。
其本人获评2022年度Nature十大人物、《麻省理工科技评论》中国区“35岁以下科技创新35人”、2022年度北京市杰出青年中关村奖、2024年“科学探索奖”,并受邀作为WHO新冠疫苗成分技术咨询小组(TAG-CO-VAC)成员、国际流行病防范创新联盟(CEPI)科学顾问。相关研究成果获评2022年度“中国科学十大进展”、2022年度“中国生命科学十大进展”。
参考文献:
https://www.nature.com/articles/s41564-025-02030-7
https://www.thelancet.com/retrieve/pii/S1473309925000155
赞一个
- 文章标签:
- 高校动态
更有众多热门




















